原发性高草酸尿症1型(PH1)新药Oxlumo(lumasiran)FDA获批
- 热度: ℃
- 来源:网络收集
- 收录时间:2020-11-25
导读:Oxlumo(lumasiran)是HAO1导向的小干扰核糖核酸(siRNA),可用于治疗1型原发性高草酸尿症(PH1),以降低儿童和成人患者的草酸尿水平。
公司: Alnylam Pharmaceuticals,Inc
.批准日期: 2020年11月23日
治疗:原发性高草酸尿症1型(PH1)
Oxlumo(lumasiran)是HAO1导向的小干扰核糖核酸(siRNA),可用于治疗1型原发性高草酸尿症(PH1),以降低儿童和成人患者的草酸尿水平。
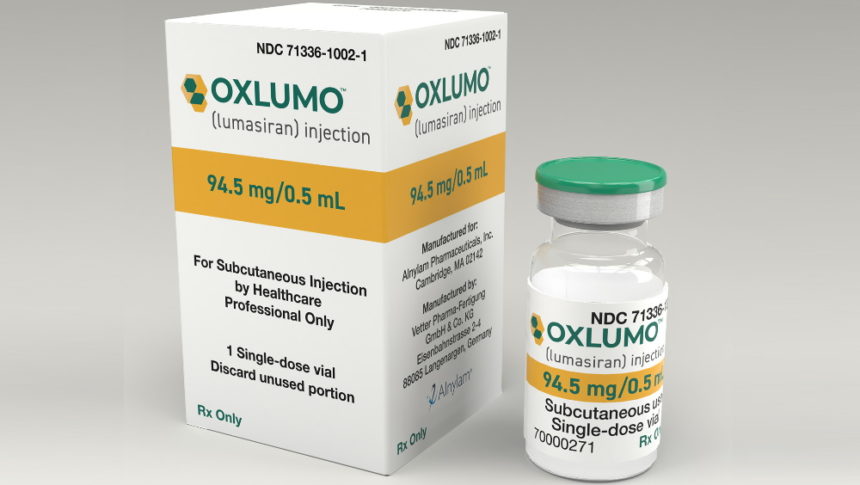
FDA批准Oxlumo(lumasiran)用于治疗1型原发性高草酸尿症
马萨诸塞州剑桥市-(美国商业资讯)-11月。2020年2月24日-领先的RNAi治疗公司Alnylam Pharmaceuticals,Inc.(Nasdaq:ALNY)今天宣布,美国食品和药物管理局(FDA)批准将Oxlumo(lumasiran)注射剂用于皮下使用,这是有史以来的第一种疗法用于治疗小儿和成年患者的原发性1型高草酸尿症(PH1),以降低草酸尿水平。PH1是一种以草酸盐过量生产为特征的超罕见遗传病。草酸盐的过量产生导致草酸钙晶体在肾脏和泌尿道中的沉积,并可能导致疼痛和复发性肾结石的形成,肾钙化,进展为肾衰竭和全身器官功能障碍。在ILLUMINATE-A(PH1有史以来最大的对照3期研究)中,Oxlumo与安慰剂相比,可显着降低草酸尿的水平,大多数患者均达到正常1或接近正常2的水平。Oxlumo展示了令人鼓舞的安全性和耐受性,其中注射部位反应(ISR)是最常见的与药物相关的不良反应。在ILLUMINATE-B儿科3期研究中,证实了Oxlumo在6岁以下患者中的安全性和有效性,结果显示尿草酸减少,总体安全性和耐受性与ILLUMINATE-A一致。Oxlumo展示了令人鼓舞的安全性和耐受性,其中注射部位反应(ISR)是最常见的与药物相关的不良反应。在ILLUMINATE-B儿科3期研究中,证实了Oxlumo在6岁以下患者中的安全性和有效性,结果显示尿草酸减少,总体安全性和耐受性与ILLUMINATE-A一致。Oxlumo展示了令人鼓舞的安全性和耐受性,其中注射部位反应(ISR)是最常见的与药物相关的不良反应。在ILLUMINATE-B儿科3期研究中,证实了Oxlumo在6岁以下患者中的安全性和有效性,结果显示尿草酸减少,总体安全性和耐受性与ILLUMINATE-A一致。
“ Oxlumo的批准进一步证明了RNAi治疗剂在改变重症,危及生命的疾病(如PH1)的治疗方面所具有的作用。ILLUMINATE-A和ILLUMINATE-B研究的结果表明,Oxlumo解决了成人,儿童和婴儿PH1的潜在病理生理问题,我们相信这种新批准的药物有可能改变这种进行性疾病的病程,” Akshay Vaishnaw说道。 ,医学博士,Alnylam研发总裁。“ Oxlumo标志着我们在不到三年的时间内获得了FDA的第三次批准,这使我们能够达到或超过Alnylam 2020战略和目标,并进一步强调了RNAi平台的生产力以及向患者带来创新药物的速度。对于受PH1影响的患者和家庭,这是一个历史性时刻,因为Oxlumo代表了他们可获得的第一个靶向治疗方案。我们感谢参加ILLUMINATE临床研究的所有研究人员,工作人员和患者,以及他们的家人,护理人员和患者倡导者。这一刻正是我们所有人所希望的。”
FDA对Oxlumo的批准主要基于随机,双盲,安慰剂对照的ILLUMINATE-A 3期研究的阳性结果,该结果于2020年6月在第57届欧洲肾脏协会–欧洲透析和移植协会虚拟大会上公布。FDA还考虑了单臂开放标签ILLUMINATE-B 3期儿科研究的积极中期结果。ILLUMINATE-B研究的主要分析结果于2020年10月在虚拟的美国肾脏病学会年会上发表。
在ILLUMINATE-A中,对39名6岁及以上,肾功能相对保留的患者(估计肾小球滤过率[eGFR]≥30 mL / min / 1.73m 2)评估了Oxlumo的疗效和安全性。)和记录的PH1诊断。该研究在全球八个国家进行,是专门针对PH1进行的最大的干预研究。患者按2:1的比例随机分配,以3 mg / kg的剂量每月接受3剂Oxlumo或安慰剂,然后每季度一次给药。研究表明,Oxlumo达到了其主要终点指标,即24小时尿草酸盐的变化百分比(校正了身体表面积,平均3到6个月)。具体而言,用Oxlumo治疗可使草酸尿的平均含量相对于基线降低65%,而据报道对安慰剂有所减少的12%,相对于安慰剂而言,平均治疗差异为53%(p = 1.7x10-14)。此外,Oxlumo在所有六个测试的次要终点上均取得了统计上显着的结果,包括达到或低于正常水平1的上限(13/25患者或52%; p = 0.001)和达到或低于正常水平2的上限1.5x(21/25患者或84%; p = 8.3 x 10-7),而接受安慰剂的患者则没有(0/13)。在初步分析期间,Oxlumo表现出令人鼓舞的安全性和耐受性,没有严重或严重的不良事件。最常见的不良反应是ISR(至少有20%的患者报告);ISR在研究期间的各个时间点发生,包括红斑,疼痛,瘙痒和肿胀。这些症状通常较轻,在注射后一天之内即可缓解,并未导致治疗中断。
在ILLUMINATE-B中,一项针对6岁以下PH1且肾功能相对保留的患者(eGFR高于45 mL / min / 1.73m2)的研究对Oxlumo进行了18例初次评估,包括三个月大的婴儿旧。根据三种体重类别(少于10千克; 10到少于20千克,以及20千克或更高)的基于体重的给药方案进行给药。在初步分析中,Oxlumo证明了从基线到第六个月(研究的第三至第六个月)尿草酸:肌酐的比例平均降低了72%。在所有三个体重类别中,草酸盐的减少是一致的。此外,Oxlumo在次要终点(包括其他草酸盐检测方法)中显示出了积极的成果。
“ PH1患者的肾功能逐渐恶化,而且通常不可避免。随着疾病的发展,终末期肾脏疾病和草酸在肾脏以外的系统性扩散的危险也在增加,危害其他器官,包括眼睛,骨骼,皮肤和心脏。这种情况,全身性草酸化,导致多器官功能障碍和死亡。病人的发病年龄,疾病进展的速度以及相关的临床表现可能因患者而异,即使是同一家庭的成员之间也是如此,这使得PH1成为诊断和治疗特别具有挑战性的疾病。直到今天,还没有批准的非手术治疗方法可以抑制PH1患者草酸盐的过度生产,肝脏移植是解决这些患者潜在的代谢缺陷的唯一先发制人的治疗方法,”西奈山克雷维斯儿童医院小儿科杰克和露西·克拉克教授兼主任,医学博士兼首席医师Jeffrey M. Saland医学博士,纽约市和ILLUMINATE-A试验的研究者。“ ILLUMMINATE-A和-B试验在成年和几个月大的成人和儿童中均证实了Oxlumo的一致疗效和安全性,并采用了不常用的给药方案,导致快速和持续减少草酸盐的产生,使Oxlumo成为一种有吸引力的治疗选择,以减少草酸盐负担,草酸盐负担是由于PH1引起的个人严重临床表现的原因。” 纽约市西奈山克雷维斯儿童医院小儿科杰克和露西·克拉克儿科肾脏病和高血压教授兼主任,ILLUMINATE-A试验的研究者。“ ILLUMMINATE-A和-B试验在成年和几个月大的成人和儿童中均证实了Oxlumo的一致疗效和安全性,并采用了不常用的给药方案,导致快速和持续减少草酸盐的产生,使Oxlumo成为一种有吸引力的治疗选择,以减少草酸盐负担,草酸盐负担是由于PH1引起的个人严重临床表现的原因。” 纽约市西奈山克雷维斯儿童医院小儿科杰克和露西·克拉克儿科肾脏病和高血压教授兼主任,ILLUMINATE-A试验的研究者。“ ILLUMMINATE-A和-B试验在成年和几个月大的成人和儿童中均证实了Oxlumo的一致疗效和安全性,并采用了不常用的给药方案,导致快速和持续减少草酸盐的产生,使Oxlumo成为一种有吸引力的治疗选择,以减少草酸盐负担,草酸盐负担是由于PH1引起的个人严重临床表现的原因。”
“受PH1影响的许多人面临持续的焦虑,这与他们病情的不可预测性有关,不确定其疾病进展的速度,以及需要进行深入透析和威胁其身体,情绪的肾脏/肝脏移植的前景和财务健康,”草酸沉着症和高草酸尿症基金会执行董事金·霍兰德(Kim Hollander)说。“ FDA对Oxlumo的批准代表了许多人的新路向,提供了有效的治疗选择和希望感。”
“ PH1从生理,情感和社会的角度对我儿子的生活产生了深远的影响。作为一个小男孩,他一直在痛苦中流失,过着无数的肾结石生活-定期经历这些结石-对身体的控制有限,错过了上学的时间,无法参加运动,艾米·鲍德斯(Amy Bowders)说,她是一个12岁男孩的母亲和照料者,被诊断患有PH1。“通过Oxlumo的批准,我们对患有PH1的患者的未来充满了希望和乐观。”
Oxlumo有望在年底前交付给美国的医疗保健提供商。
FDA在优先审查中对Oxlumo进行了审查,以前已被授予突破性疗法,孤儿药和罕见儿科疾病称号。在Oxlumo的批准下,FDA已向Alnylam授予了小儿罕见病优先审阅凭单,使该公司有权指定单个新药申请,以便将来有资格进行优先审阅。11月19日,在人类使用药品委员会(CHMP)给予积极评价后,欧洲委员会授予Oxlumo用于所有年龄段的PH1治疗的销售许可。Lumasiran先前曾获得欧洲药品管理局(EMA)的优先药品(PRIME)称号以及欧盟的孤儿称号。EMA还授予Lumasiran加速评估,
在正在进行的ILLUMINATE-C 3期临床试验中,也正在评估Oxlumo的安全性和有效性,该试验适用于所有年龄在晚期PH1的患者,包括接受透析的患者。ILLUMINATE研究共同组成了一项全面的临床开发计划,旨在证明Oxlumo在诊断为PH1的所有患者中的安全性和有效性。
1正常值定义为草酸尿素水平等于或低于正常上限(ULN;≤0.514 mmol / 24 hr / 1.73 m 2)。
2近乎正常的定义为草酸尿素水平等于或低于1.5 x ULN(≤0.771 mmol / 24 hr / 1.73 m 2)
重要安全信息
不良反应
Oxlumo治疗的患者中最常见的不良反应是注射部位反应(38%)。症状包括红斑,疼痛,瘙痒和肿胀。
怀孕和哺乳期
没有关于Oxlumo在孕妇中使用的数据。没有关于母乳中Oxlumo的存在或其对母乳喂养婴儿或产奶量的影响的数据。考虑母乳喂养对发育和健康的好处,以及母亲对Oxlumo的临床需求以及Oxlumo或潜在的母体状况对母乳喂养的孩子的任何潜在不利影响。
有关Oxlumo的其他信息,请参阅完整的处方信息。
关于Oxlumo™(lumasiran)
Oxlumo是一种靶向羟基酸氧化酶1(HAO1)的RNAi治疗药物,可用于治疗1型原发性高草酸尿症(PH1),以降低儿童和成人患者的草酸尿水平。HAO1编码乙醇酸氧化酶(GO),这是PH1中引起疾病的缺陷的上游酶。Oxlumo通过降解HAO1信使RNA并减少GO的合成来发挥作用,GO的合成可抑制肝中草酸盐的产生,草酸盐是负责PH1临床表现的有毒代谢产物。在关键的ILLUMINATE-A研究中,与安慰剂相比,Oxlumo被证明可以显着降低草酸尿的水平,大多数患者达到正常或接近正常水平。注射部位反应(ISR)是最常见的药物相关不良反应。在ILLUMINATE-B儿科3期研究中,Oxlumo具有与ILLUMINATE-A一致的功效和安全性。Oxlumo利用Alnylam的增强稳定化学(ESC)-GalNAc共轭技术来提高效能和耐用性。Oxlumo每月一次皮下注射,持续三个月,然后每季度一次,以实际体重为基础。对于体重不足10公斤的患者,仍需每月继续服用。Oxlumo应该由医疗保健专业人员管理。有关Oxlumo的更多信息,请访问OXLUMO.com。然后每季度一次,以实际体重为基准。对于体重不足10公斤的患者,仍需每月继续服用。Oxlumo应该由医疗保健专业人员管理。有关Oxlumo的更多信息,请访问OXLUMO.com。然后每季度一次,以实际体重为基准。对于体重不足10公斤的患者,仍需每月继续服用。Oxlumo应该由医疗保健专业人员管理。有关Oxlumo的更多信息,请访问OXLUMO.com。
关于1型原发性高草酸尿症(PH1)
PH1是一种超罕见的遗传病,在美国和欧洲,每百万人口中估计有1-3个人受到影响。PH1的特征是肝脏中草酸盐的过量生产。过量的草酸盐会导致草酸钙晶体在肾脏和泌尿道中沉积,并可能导致疼痛和复发性肾结石和肾钙化病的形成。肾损伤是由草酸盐引起的肾小管毒性,肾脏中草酸钙的沉积以及草酸钙结石引起的尿路阻塞引起的。PH1与肾功能的逐步下降有关,由于过量的草酸盐不再能有效排泄,加剧了疾病的发展,导致草酸盐在骨骼,眼睛,皮肤和心脏中的积累和沉积,从而导致严重的疾病和死亡。 。迄今为止,管理选择仅限于水合作用,结晶抑制剂,以及在少数具有特定基因型的患者中,吡ido醇(维生素B6)。这些措施不能充分解决草酸盐的过度生产,但有助于延缓不可避免的肾衰竭进展,并需要进行深入透析以作为肝/肾双重或顺序移植的桥梁。肝移植是解决潜在代谢缺陷的唯一干预措施,但与高发病率和高死亡率以及终身免疫抑制相关。直到今天,还没有批准的PH1药物疗法。这些措施不能充分解决草酸盐的过度生产,但有助于延缓不可避免的肾衰竭进展,并需要进行深入透析以作为肝/肾双重或顺序移植的桥梁。肝移植是解决潜在代谢缺陷的唯一干预措施,但与高发病率和高死亡率以及终身免疫抑制相关。直到今天,还没有批准的PH1药物疗法。这些措施不能充分解决草酸盐的过度生产,但有助于延缓不可避免的肾衰竭进展,并需要进行深入透析以作为肝/肾双重或顺序移植的桥梁。肝移植是解决潜在代谢缺陷的唯一干预措施,但与高发病率和高死亡率以及终身免疫抑制相关。直到今天,还没有批准的PH1药物疗法。
关于RNAi
RNAi(RNA干扰)是基因沉默的自然细胞过程,代表了当今生物学和药物开发中最有前途和最迅速发展的领域之一。它的发现被誉为“每十年左右发生一次的重大科学突破”,并获得2006年诺贝尔生理学或医学奖。通过利用RNAi在我们细胞中发生的自然生物学过程,一种新的称为RNAi治疗剂的药物现已成为现实。小干扰RNA(siRNA)是介导RNAi的分子,并构成Alnylam的RNAi治疗平台,它们通过有效沉默信使RNA(mRNA)(遗传前体)来编码当今疾病的上游,信使RNA(mRNA)编码引起疾病或疾病的途径蛋白 从而阻止了它们的制造。这是一种革命性的方法,具有改变遗传病和其他疾病患者护理的潜力。
关于Alnylam制药
Alnylam(Nasdaq:ALNY)正在将RNA干扰(RNAi)的翻译转变为一类崭新的创新药物,有可能改变受罕见遗传,心脏代谢,肝感染和中枢神经系统困扰的人们的生活( CNS)/眼部疾病。基于诺贝尔奖的科学,RNAi疗法代表了一种强大的,经过临床验证的方法,可用于治疗各种严重的衰弱性疾病。Alnylam成立于2002年,致力于通过强大的RNAi治疗平台实现将科学可能性变为现实的大胆愿景。Alnylam的商业RNAi治疗产品为ONPATTRO®(patisiran),GIVLAARI®(givosiran)和OXLUMO™(lumasiran)。Alnylam有大量的研究药物,包括处于后期开发阶段的六个候选产品。Alnylam正在执行其“ Alnylam 2020”战略,该战略将建立一个多产品,商业阶段的生物制药公司,该公司具有基于RNAi的药物的可持续生产渠道,以满足治疗选择有限或不足的患者的需求。Alnylam总部位于马萨诸塞州剑桥。