脊髓性肌萎缩(SMA)新药Evrysdi(risdiplam)口服液
- 热度: ℃
- 来源:网络收集
- 收录时间:2020-08-21
导读:Evrysdi(risdiplam)是运动神经元2(SMN2)拼接修饰剂的存活,可用于治疗2个月及以上的患者的脊髓性肌萎缩(SMA)。
公司: Genentech,Inc
.批准日期: 2020年8月7日
治疗:脊髓性肌萎缩症
Evrysdi(risdiplam)是运动神经元2(SMN2)拼接修饰剂的存活,可用于治疗2个月及以上的患者的脊髓性肌萎缩(SMA)。
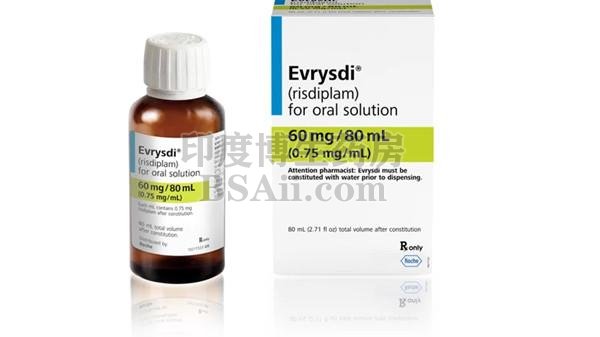
加利福尼亚州南旧金山-2020年8月7日-罗氏集团成员Genentech今天宣布,美国食品药品监督管理局(FDA)批准了Evrysdi(risdiplam)用于治疗脊髓性肌萎缩症(SMA)。成人和2个月以上的儿童。Evrysdi在两个年龄和疾病严重程度不同的人(包括1型,2型和3型SMA)的两项临床试验中显示出运动功能的临床意义改善。婴儿能够在没有支撑的情况下坐至少5秒钟,这是该疾病自然过程中通常没有的关键运动里程碑。与自然病史相比,Evrysdi在没有永久通气的情况下在12和23个月时也提高了生存率。液体药物Evrysdi每天在家中通过口或饲管给药。
医学博士Levi Garraway博士说:“鉴于美国大部分SMA患者仍未得到治疗,我们相信Evrysdi凭借其良好的临床表现和口服给药,可能为许多患有这种罕见神经疾病的患者带来有意义的益处。” ,首席医学官兼全球产品开发主管。“ SMA社区的力量和决心不断激励着我们,这是我们为SMA开发的首款药物,因此今天我们与他们一起庆祝我们的集体成就。”
作为SMA一项庞大而强大的临床试验计划的一部分,正在对450多人进行Evrysdi研究。该计划包括2个月大的婴儿至60岁的具有不同症状和运动功能的婴儿,例如脊柱侧弯或关节挛缩症患者,以及以前接受过另一种药物治疗SMA的婴儿。该批准基于两项旨在代表广泛的SMA患者的临床研究的数据:FIREFISH用于2至7个月大的有症状婴儿;和2至25岁的儿童和成人中的SUNFISH。SUNFISH是第一个也是唯一一个包含2型和3型SMA成人的安慰剂对照试验。
在FIREFISH中,按照贝利婴儿和幼儿发展量表第三版(BSID-III)的标准,接受治疗剂量治疗的婴儿中有41%(7/17)能够坐下至少5秒钟,而无需支撑。此外,有90%(19/21)的婴儿在治疗12个月时没有永久通气,并且年龄在15个月以上。如未经治疗的婴儿发作性SMA的自然史中所述,预计婴儿无法独立坐下,只有14%的婴儿在没有永久通气的情况下可以存活超过14个月。在SUNFISH中,接受Evrysdi治疗的儿童和成人在12个月时运动功能的临床意义和统计学显着改善(平均差异1.55点; p = 0.0156)与安慰剂相比(1.36分[95%CI:0.61、2.11]) ; -0。
Evrysdi在FIREFISH和SUNFISH试验中建立了良好的疗效和安全性。最常见的不良反应是后来发作的SMA发烧,腹泻和皮疹。在婴儿发作的SMA中,最常见的不良事件类似,还包括上呼吸道感染,肺炎,便秘和呕吐。没有与治疗相关的安全性发现可导致退出两项研究。
Cure SMA总裁肯尼思·霍比(Kenneth Hobby)表示:“一生中,许多SMA人可能会失去执行关键动作的能力,这可能会影响独立参与日常生活各方面甚至改变生活的能力。” “对Evrysdi的批准是我们社区期待已久的里程碑。我们赞赏Genentech承诺在其临床试验计划中反映现实世界中SMA人群的全部范围,并开发出可以在家中使用的治疗方法。”
Evrysdi设计用于通过增加运动神经元(SMN)蛋白存活的产生来治疗SMA。SMN蛋白遍布全身,对于维持健康的运动神经元和运动至关重要。作为与SMA Foundation和PTC Therapeutics合作的一部分,Genentech领导Evrysdi的临床开发。
Evrysdi将在两周内在美国上市,可以通过Express Scripts专业药房Accredo Health Group Inc.直接运送到患者家中。
Genentech致力于帮助患者使用其医师开具的药物。对于SMA患者,MySMA支持计划团队可以回答问题,提供产品教育并帮助家庭了解保险范围,并导航适当的财务援助选项以开始并继续使用Evrysdi。
关于埃夫里迪(risdiplam)
Evrysdi是运动神经元2(SMN2)剪接修饰剂的存活,其设计用于治疗由5q号染色体中导致SMN蛋白缺陷的突变引起的SMA。Evrysdi每天在家中以液体形式通过口或饲管给药。
Risdiplam在2018年获得了欧洲药品管理局(EMA)的PRIME称号,并在2017年和2019年分别获得了FDA和EMA的孤儿药称号。目前,risdiplam已在巴西,智利,中国,印度尼西亚,俄罗斯,韩国和台湾备案。即将向Evrysdi的EMA提交营销授权申请(MAA)。
关于关键研究
芬兰语(NCT02913482)
FIREFISH是一项开放式,分为两部分的关键性研究,旨在评估1至7个月大的1型SMA患者的Evrysdi安全性,耐受性,疗效,药代动力学(PK)和药效学(PD)。第1部分评估了几种Evrysdi剂量,并确定第2部分的治疗剂量为0.2 mg / kg。在第1部分中,Evrysdi治疗12个月后:
用BSID-III总体运动量表测得,接受治疗剂量治疗的婴儿中有41%(7/17)能够在无支撑的情况下坐下至少5秒钟。
在所有婴儿中,有90%(19/21)存活而没有永久通气*,并且达到15个月以上。
所有患者中有81%(17/21)在经过至少23个月的治疗后存活,没有永久通气*,并且年龄达到28个月或更大(中位数32个月;范围为28到45个月)。
*永久通气定义为气管切开术或每天无创通气≥16小时或在无急性可逆事件发生或解决后连续插管≥21天。
SUNFISH(NCT02908685)
SUNFISH是一项分为两部分的安慰剂对照多中心枢纽试验,旨在评估2至25岁的2型或3型SMA患者(包括脊柱侧弯患者)的Evrysdi安全性,耐受性,疗效,PK和PD(第2部分占67%) )和基准关节挛缩。在第2部分中,经过12个月的治疗,Evrysdi的治疗导致:
与安慰剂组(1.36)相比,在12个月时,MFM-32总评分的基线变化(1.55点平均差异; p = 0.0156)从基线的变化衡量,儿童和成人的运动功能具有临床意义和统计学意义上的显着改善得分[95%CI:0.61、2.11];-0.19分[95%CI:1.22、0.84]。MFM-32评估了SMA患者的32种不同的运动功能。
与基线相比,上肢运动功能得到了改善,这是通过修订的上肢模块(RULM)进行的,该模型是研究的次要独立运动功能终点(差异为1.59; p = 0.0028)。
重要审判安全数据
Evrysdi的安全性是在FIREFISH和SUNFISH关键试验中建立的。迟发性SMA(发生至少10%的Evrysdi治疗的患者发生率最高,且比对照组多发生)的最常见不良反应是发烧,腹泻和皮疹。婴儿期SMA中最常见的不良反应与后期SMA患者中观察到的相似。此外,最常见的不良反应(发生率至少为10%)是上呼吸道感染,肺炎,便秘和呕吐。
关于Evrysdi临床试验计划
除了FIREFISH和SUNFISH,Evrysdi还被广泛的SMA患者评估,包括:
JEWELFISH(NCT03032172):一项开放性探索性试验,旨在评估6个月至60岁年龄在接受其他研究或批准的SMA治疗至少90的SMA患者的安全性,耐受性,药代动力学(PK)和药效学(PD)在收到Evrysdi之前的几天。这项研究的招募已经完成,共有174人参加。
RAINBOWFISH(NCT03779334):一项开放标签,单臂,多中心研究,调查从出生到六周龄(初剂量)Evrysdi对婴儿(〜n = 25)的有效性,安全性,药代动力学和药效学,从出生到六周诊断出尚未出现症状的SMA。该研究正在招募中。
关于SMA
SMA是一种严重的进行性神经肌肉疾病,可能致命。它影响约10,000个婴儿中的一个,是婴儿死亡率的主要遗传原因。SMA是由存活运动神经元1(SMN1)基因的突变引起的,该突变导致SMN蛋白的缺乏。这种蛋白质遍布全身,对控制肌肉和运动的神经功能至关重要。没有它,神经细胞将无法正常运作,随着时间的推移导致肌肉无力。根据SMA的类型,个人的体力以及步行,进食或呼吸的能力可能会大大降低或丧失。
什么是Evrysdi?
Evrysdi是一种处方药,用于治疗2个月及以上的成人和儿童的脊髓性肌萎缩症(SMA)。
尚不知道Evrysdi在2个月以下的儿童中是否安全有效。
重要安全信息
服用Evrysdi之前,患者应将其所有医疗状况告知医疗保健提供者,包括是否:
有肝脏问题
正在怀孕或打算怀孕。如果患者已怀孕或计划怀孕,则应在服药之前向医疗保健提供者咨询。Evrysdi可能会伤害未出生的婴儿。
是可以怀孕的女人:
在患者开始使用Evrysdi治疗之前,其医疗保健提供者可能会测试他们是否怀孕。由于Evrysdi可能会伤害未出生的婴儿,因此医疗保健提供者将决定在这段时间内服用Evrysdi是否适合他们
患者应与医疗保健提供者讨论可能适合他们的节育方法。患者应在治疗期间以及停止Evrysdi后至少1个月内使用节育措施
是打算生育孩子的成年男性:Evrysdi可能会影响男人生育孩子的能力(生育力)。如果患者对此感到担忧,则应确保向医疗保健提供者咨询
正在母乳喂养或计划母乳喂养。尚不知道Evrysdi是否会进入母乳并可能伤害婴儿。如果患者计划母乳喂养,则应与医疗保健提供者讨论在用Evrysdi治疗时喂养婴儿的最佳方法
患者应将其服用的所有药物告知医疗保健提供者,包括处方药和非处方药,维生素和草药补品。患者应保留一份清单,以在获得新药时向医疗保健提供者和药剂师展示
患者应从药房接受Evrysdi的液体,可以口服或通过饲管服用。液体溶液由患者的药剂师准备。如果瓶中的药物是粉末,请勿使用。患者应联系药剂师进行更换
避免使Evrysdi沾在皮肤上或眼睛中。如果Evrysdi沾到皮肤上,请用肥皂和水清洗该区域。如果Evrysdi进入眼睛,请用水冲洗眼睛
Evrysdi最常见的副作用包括:
对于以后发作的SMA:
发热
腹泻
皮疹
对于小儿发作性SMA:
发热
腹泻
皮疹
流鼻涕,打喷嚏,喉咙痛和咳嗽(上呼吸道感染)
肺部感染
便秘
呕吐
这些并不是Evrysdi的所有可能的副作用。有关Evrysdi的风险和收益状况的更多信息,患者应咨询其医疗保健提供者或药剂师。
请参阅完整的处方信息以获取其他重要安全信息。
关于Genentech在神经科学中
神经科学是Genentech和Roche的研发重点。我们的目标是追求开创性的科学,以开发有助于改善患有慢性和潜在毁灭性疾病的人们的生活的新疗法。
Genentech和罗氏(Roche)正在研究多种神经疾病的药物,包括多发性硬化症,中风,视神经脊髓炎频谱疾病,阿尔茨海默氏病,亨廷顿舞蹈病,帕金森氏病,杜兴氏肌营养不良症和自闭症谱系障碍。与我们的合作伙伴一起,我们致力于突破科学理解的界限,以解决当今神经科学中一些最困难的挑战。
关于基因泰克
Genentech成立于40年前,是一家领先的生物技术公司,致力于发现,开发,生产和商业化用于治疗患有严重威胁生命的患者的药物。该公司是罗氏集团的成员,总部位于加利福尼亚州南旧金山。
资料来源:Genentech
发表于:2020年8月