重症肌无力新药Vyvgart(efgartigimod alfa-fcab)注射液FDA获批
- 热度: ℃
- 来源:网络收集
- 收录时间:2021-12-21
导读:Vyvgart (efgartigimod alfa-fcab) 是一种新生儿 Fc 受体阻滞剂,适用于治疗抗乙酰胆碱受体 (AChR) 抗体阳性的成人全身性重症肌无力 (gMG)。
公司: argenx SE
批准日期: 2021 年 12 月 17 日
治疗:重症肌无力
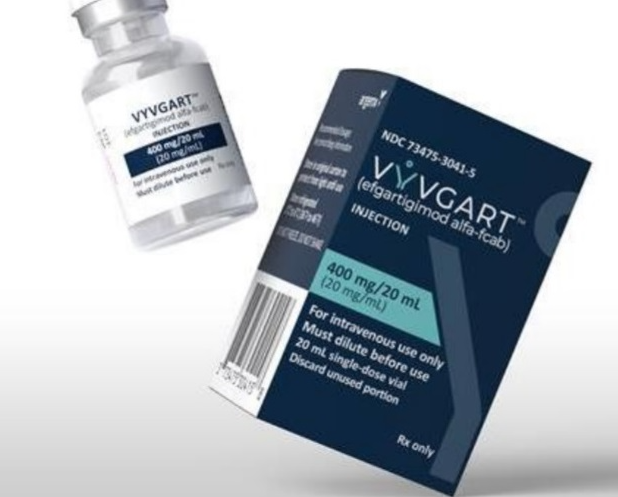
Vyvgart (efgartigimod alfa-fcab) 是一种新生儿 Fc 受体阻滞剂,适用于治疗抗乙酰胆碱受体 (AChR) 抗体阳性的成人全身性重症肌无力 (gMG)。
(FDA)已批准 Vyvgart(efgartigimod alfa-fcab) 用于治疗抗乙酰胆碱受体 (AChR) 抗体阳性的成人全身性重症肌无力 (gMG)。这些患者约占 gMG 总人口1 的85% 。凭借这一监管里程碑,Vyvgart 是第一个也是唯一一个获得 FDA 批准的新生儿 Fc 受体(FcRn)阻滞剂。
“今天是 argenx 和 gMG 社区新时代的开始,因为我们兑现了为患有这种使人衰弱的疾病的人们提供创新治疗方案的承诺。Vyvgart 的批准代表了许多成就:我们的第一个获批产品;首个也是唯一一个获得 FDA 批准的新生儿 Fc 受体阻滞剂;argenx 首席执行官 Tim Van Hauwermeiren 说:“这是第一个批准的旨在减少致病性 IgG 的疗法,这是 gMG 的潜在驱动因素。” “重要的是,我们要感谢参与 ADAPT 试验的患者、支持性护理人员、研究人员和研究团队,以及我们的合作伙伴和敬业的员工的辛勤工作和协作——他们使这一里程碑成为可能。
“我们积极进取的商业团队已被激活并准备为患者提供 Vyvgart。我们相信自身免疫领域正处于进化的边缘,我们希望这将是众多 Vyvgart 发布中的第一个,让我们能够帮助改善世界各地患者的生活,”Van Hauwermeiren 先生继续说道。
全身性重症肌无力是一种罕见的慢性神经肌肉疾病,其特征是使人虚弱和可能危及生命的肌肉无力。Vyvgart 是一种人类 IgG1 抗体片段,可与 FcRn 结合,导致循环免疫球蛋白 G (IgG) 抗体减少。AChR 自身抗体在神经肌肉接头处的作用是 gMG 2的关键驱动因素。
“gMG 社区一直在等待 FDA 批准 Vyvgart,特别是对于那些在说话、咀嚼和吞咽食物、刷牙和头发等基本个人任务上挣扎的患者,在某些严重的情况下,还有呼吸,”萨曼莎·马斯特森评论道。 ,美国重症肌无力基金会主席兼首席执行官。“我们感谢 argenx 对 gMG 患者社区的持续承诺,这使他们能够提供这种急需的新治疗方案,并有可能改变许多 gMG 患者的生活。”
经证实的临床疗效和安全性
“患有 gMG 的人一直需要针对该疾病的潜在发病机制并得到临床数据支持的新治疗方案,”医学博士、神经病学(神经肌肉疾病)、医学和医学教授 James F. Howard Jr. 说。北卡罗来纳大学教堂山医学院神经病学系 Allied Health 和 ADAPT 试验的首席研究员。“今天的批准代表了受这种使人衰弱的疾病影响的 gMG 患者和家庭的一个重要的新进展。这种疗法有可能减轻 gMG 的疾病负担并改变我们治疗这种疾病的方式。”
Vyvgart 的批准基于全球第 3 期 ADAPT 试验的结果,该试验发表在 2021 年 7 月的The Lancet Neurolog 上。ADAPT 试验达到了其主要终点,表明与安慰剂相比,在接受 Vyvgart 治疗后,在 MG-ADL 量表上明显更多的抗 AChR 抗体阳性 gMG 患者是应答者(68% 对 30%;p<0.0001)。反应者被定义为在第一个治疗周期中连续四周或更长时间在 MG-ADL 量表上至少降低两点。
与安慰剂相比,Vyvgart 治疗后定量重症肌无力 (QMG) 量表上的应答者明显更多(63% 对 14%;p<0.0001)。反应者被定义为在第一个治疗周期中连续四个星期或更长时间在 QMG 量表上至少降低三分。
Vyvgart 在 ADAPT 临床试验中具有证明的安全性。ADAPT 中最常见的不良事件是呼吸道感染(33% 对 29% 安慰剂)、头痛(32% 对 29% 安慰剂)和尿路感染(10% 对 5% 安慰剂)。
访问和我的 Vyvgart 路径
argenx 致力于支持负担得起的 Vyvgart 访问。作为这一承诺的一部分,argenx 正在推出My Vyvgart Path,该计划旨在在整个治疗过程中将患者和临床医生与个性化支持联系起来。计划资源包括疾病和产品教育、获取支持和福利验证以及针对符合条件的患者的财务援助计划。
患有 gMG 的成年人每个人都会经历不同的疾病过程,从而导致疾病严重程度和对治疗反应的可变性。argenx 优先考虑与主要付款人的早期积极接触,以解决有关更广泛预算可预测性的问题。公司已与多家国家和地区商业支付方达成原则协议,以构建基于价值的协议。这些协议旨在为付款人提供成本的可预测性,并为患者提供适当的访问权限。
“全身性重症肌无力给患者、家庭和整个医疗保健系统带来了沉重的生活方式和治疗负担。这种自身免疫性疾病对每位患者的影响不同,这可能会导致剂量和每位患者产生的成本发生变化,”信诺公司执行副总裁兼首席临床官 Steve Miller 医学博士说。“Vyvgart 的批准有望解决治疗差距患有这种疾病的患者。argenx 提出了一种创新的、基于价值的合同方法,这将帮助支付方在面临确保现实世界剂量仍然负担得起的挑战时具有成本可预测性。这是 argenx 和 Evernorth 之间早期接触导致批准的直接结果。
efgartigimod 用于治疗 gMG 的上市许可申请目前正在接受日本药品和医疗器械管理局 (PMDA) 和欧洲药品管理局 (EMA) 的审查,预计每个机构将在 2022 年第一季度和下半年做出决定.
argenx 与 Zai Lab 就 efgartigimod 在大中华区的开发和商业化签订了独家合作协议。Zai Lab 有望在 2022 年年中之前在大中华区申请批准。根据与 Zai Lab 的战略协议条款,在美国批准 Vyvgart 后,argenx 将获得 2500 万美元的里程碑付款。此外, argenx 与 Medison 建立了独家合作伙伴关系,以在以色列 gMG 中实现 efgartigimod 的商业化。Medison 有望于 2022 年第二季度在以色列申请批准。
有关其他信息,请参阅下面的重要安全信息和完整的处方信息。
重要安全信息
什么是 Vyvgart (efgartigimod alfa-fcab)?
Vyvgart 是一种处方药,用于治疗称为全身性重症肌无力的病症,这种病症会导致全身肌肉容易疲倦和虚弱,对于针对乙酰胆碱受体蛋白的抗体呈阳性的成年人(抗 AChR 抗体阳性)。
关于 Vyvgart,我应该了解哪些最重要的信息?
Vyvgart 可能会导致严重的副作用,包括:
感染。 Vyvgart 可能会增加感染的风险。在一项临床研究中,最常见的感染是尿路和呼吸道感染。Vyvgart 与安慰剂相比,更多患者的白细胞计数、淋巴细胞计数和中性粒细胞计数低于正常水平。大多数感染和血液副作用的严重程度为轻度至中度。您的医疗保健提供者应在开始治疗前、治疗期间和使用 Vyvgart 治疗后检查您是否有感染。如果您有任何感染史,请告诉您的医疗保健提供者。如果您在 Vyvgart 治疗期间出现感染的迹象或症状,例如发烧、发冷、尿频和/或疼痛、咳嗽、疼痛和鼻腔/鼻窦阻塞、喘息、呼吸急促、疲劳,喉咙痛,
不良免疫反应(超敏反应)。Vyvgart 会导致免疫系统出现不良反应,例如皮疹、皮下肿胀和呼吸急促。在临床研究中,反应为轻度或中度,发生在给药后 1 小时至 3 周内,且这些反应未导致 Vyvgart 停药。您的医疗保健提供者应在治疗期间和治疗后对您进行监测,并在需要时停用 Vyvgart。立即告诉您的医疗保健提供者任何不良反应。
在服用 Vyvgart 之前,请告诉您的医疗保健提供者您的所有医疗状况,包括如果您:
有感染史或您认为自己感染了
已接种或计划接种疫苗(免疫接种)。与您的医疗保健提供者讨论您是否需要在开始新的 Vyvgart 治疗周期之前接受适合年龄的免疫接种。尚未研究在 Vyvgart 治疗期间使用疫苗,并且活疫苗或减毒活疫苗的安全性未知。在使用 Vyvgart 治疗期间不建议接种活疫苗或减毒活疫苗。
怀孕或计划怀孕并且正在母乳喂养或计划母乳喂养。
告诉您的医疗保健提供者您服用的所有药物,包括处方药和非处方药、维生素和草药补充剂。
Vyvgart 的常见副作用是什么?
Vyvgart 最常见的副作用是呼吸道感染、头痛和尿路感染。
这些并不是 Vyvgart 的所有可能的副作用。打电话给您的医生,征求有关副作用的医疗建议。
请查看 Vyvgart 的完整处方信息并咨询您的医生。
关于第 3 阶段 ADAPT 试验
第三阶段 ADAPT 试验是一项为期 26 周的随机、双盲、安慰剂对照、多中心、全球试验,评估 Vyvgart 在成年 gMG 患者中的安全性和有效性。北美、欧洲和日本共有 167 名成年 gMG 患者参加了该试验。除了稳定剂量的当前 gMG 治疗外,患者以 1:1 的比例随机接受 Vyvgart 或安慰剂。ADAPT 旨在实现个性化的治疗方法,包括初始治疗周期,然后是基于临床评估的后续治疗周期。主要终点是 Vyvgart 和安慰剂治疗组在第一个治疗周期中抗 AChR 抗体阳性人群中 MG-ADL 应答者百分比的比较。
关于 Vyvgart
Vyvgart (efgartigimod alfa-fcab) 是一种人类 IgG1 抗体片段,可与新生儿 Fc 受体 (FcRn) 结合,导致循环 IgG 减少。它是第一个也是唯一一个获批的 FcRn 阻滞剂。Vyvgart 在美国被批准用于治疗患有全身性重症肌无力 (gMG) 的成人,他们的抗 AChR 抗体呈阳性。
关于全身性重症肌无力
全身性重症肌无力 (gMG) 是一种罕见的慢性自身免疫性疾病,其中 IgG 自身抗体会破坏神经和肌肉之间的通讯,导致衰弱和可能危及生命的肌肉无力。大约 85% 的 MG 患者在 24 个月内发展为 gMG 1,全身肌肉可能会受到影响。具有确认的 AChR 抗体的患者约占 gMG 总人口1 的85% 。
关于 argenx
argenx 是一家全球免疫学公司,致力于改善患有严重自身免疫性疾病和癌症的人们的生活。argenx 通过其免疫学创新计划 (IIP) 与领先的学术研究人员合作,旨在将免疫学突破转化为世界一流的新型抗体药物组合。argenx 开发并将商业化第一个也是唯一一个 FDA 批准的新生儿 Fc 受体阻滞剂 Vyvgart(efgartigimod alfa-fcab),用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人 gMG 患者。公司正在评估 efgartigimod 在多种严重自身免疫疾病中的疗效,并在其治疗特许经营权内推进几种早期实验药物。