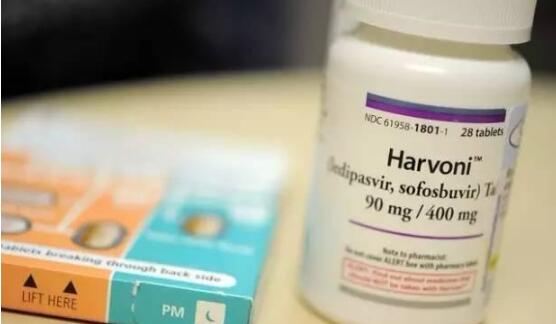
Trikafta(elexacaftor / tezacaftor / ivacaftor和ivacaftor)是一种三联疗法,用于治疗12岁及以上且囊性纤维化跨膜电导调节剂(CFTR)中至少有F508del突变拷贝的患者的囊性纤维化(CF)。)基因。
波士顿-(美国商业资讯)-十月 2019年21月21日-顶点药物公司(Nasdaq:VRTX)今天宣布,美国食品药品监督管理局(FDA)已批准Trikafta(elexacaftor / tezacaftor / ivacaftor和ivacaftor)用于治疗囊性纤维化(CF)在12岁及以上的人群中,其在囊性纤维化跨膜电导调节剂(CFTR)基因中具有至少一个F508del突变,这是最常见的导致CF的突变。有了此批准,大约有6,000名12岁及12岁以上CF人群中有一个F508del突变和一个最小功能突变(F / MF)的药物针对了其CF的根本原因。此外,目前约有12,000名具有一或两个F508del突变的人符合Vertex的其他三种FDA批准的CF药物之一的资格,现在也符合Trikafta的资格。
今天是CF患者,他们的家人和Vertex的里程碑。经过20年的共同努力,我们已获得FDA批准的Trikafta:一种突破性的药物,有可能在未来治疗多达90%的CF患者。对于美国大约6,000名患有CF的人来说,Trikafta是第一种可以治疗疾病根本原因的药物。” Vertex董事长,总裁兼首席执行官Jeffrey Leiden博士说。“我要亲自感谢从事此计划近20年的数百名Vertex科学家-他们中的许多人全职致力于改变这种疾病的病程;CF基金会在整个旅程中提供了支持,鼓励和帮助;最重要的是成千上万的患者,护理人员,
Gregory Fleming James囊性纤维化研究中心主任史蒂文·罗说:“今天的批准是囊性纤维化治疗的一个历史性时刻,有可能使更多的人受益于CFTR调节剂疗法来治疗其疾病的基本缺陷。”阿拉巴马大学伯明翰分校。“在临床试验中,Trikafta通常耐受性良好,并证明CF的多种预后指标有所改善,包括FEV1的改善,呼吸道症状的改善,以及在24周的F / MF研究中,肺部加重的发生率降低了, BMI。”
医学博士Reshma Kewalramani博士说:“批准的惊人速度突显了我们与FDA和CF社区的共同紧迫感,即将这种药物带给具有CF资格的合格人群,尤其是那些没有针对其疾病根本原因的药物的人群,” Vertex全球药品开发和医疗事务执行副总裁兼首席医疗官。“我们仍然致力于为所有患有这种疾病的人不懈地追求转化疗法的发展。”
Vertex已向欧洲药品管理局(EMA)提交了营销许可申请(MAA),以进行elexacaftor / tezacaftor / ivacaftor联合治疗方案。Vertex目前正在进行一项3期研究,正在评估具有F / MF和F / F CF突变的6至11岁人群的elexacaftor / tezacaftor / ivacaftor,并致力于评估6岁以下儿童的elexacaftor / tezacaftor / ivacaftor。计划的未来研究。
有关Vertex的患者援助计划的更多信息,请访问VertexGPS.com。
关于特里卡夫塔
Trikafta(elexacaftor / tezacaftor / ivacaftor和ivacaftor)是一种处方药,用于治疗12岁以上的患者,其囊性纤维化跨膜电导调节剂(CFTR)中至少有F508del突变的一个副本)基因。患者应咨询医生,以了解他们是否具有指定的CF基因突变。目前尚不清楚Trikafta对12岁以下的儿童是否安全有效。Trikafta被设计用来增加F508del-CFTR蛋白在细胞表面的数量和功能。Trikafta的批准得到两项针对12岁以上CF患者的全球3期全球研究的积极结果的支持:
帮助患者使用Trikafta
在Vertex工作的人们都知道,药物只能帮助可以得到药物的人们。“ Vertex指导和患者支持(Vertex GPS™)”计划提供了一个由Vertex员工组成的团队,这些团队致力于帮助在美国开出处方我们的药物的合格人员了解其保险利益以及可用来帮助他们的资源。
Vertex还为有商业保险范围的合格人员提供共付额援助计划,并为符合某些收入和其他资格标准的合格人员提供免费药物计划。有关更多信息,请访问www.VertexGPS.com或致电1-877-752-5933。
关于囊性纤维化
囊性纤维化(CF)是一种罕见的,缩短生命的遗传病,全世界约有75,000人受到感染。CF是一种累进的多系统疾病,会影响肺,肝,胃肠道,鼻窦,汗腺,胰腺和生殖道。CF是由CFTR基因中的某些突变导致的CFTR蛋白缺陷和/或缺失引起的。孩子必须继承两个有缺陷的CFTR基因-每个父母都有一个-才能获得CF。尽管有多种不同类型的CFTR突变可导致该疾病,但绝大多数CF患者中至少有一个F508del突变。这些突变可以通过基因测试或基因分型测试确定,通过在细胞表面产生无效的和/或过少的CFTR蛋白来导致CF。CFTR蛋白的功能缺陷和/或缺失会导致盐和水流入和流出许多器官中的细胞的能力较差。在肺部,这会导致异常粘稠的粘液堆积,这些粘液会导致慢性肺部感染和许多患者进行性肺损伤,最终导致死亡。中位死亡年龄在30年代初。
TRIKAFTA的适应症和重要安全信息(elexacaftor / tezacaftor / ivacaftor和ivacaftor)片剂
Trikafta是一种处方药,用于治疗12岁以上且至少有一个F508del突变拷贝的患者的囊性纤维化(CF)。囊性纤维化跨膜电导调节剂(CFTR)基因。患者应咨询医生,以了解他们是否具有指定的CF基因突变。目前尚不清楚Trikafta对12岁以下的儿童是否安全有效。
如果患者服用某些药物,则不应服用Trikafta,例如:利福平或利福布汀等抗生素;癫痫发作药物,如苯巴比妥,卡马西平或苯妥英钠;圣约翰草。
在服用Trikafta之前,患者应告知医生所有医疗状况,包括是否患有:肾脏问题,有或曾经有肝脏问题,怀孕或计划怀孕,因为尚不清楚Trikafta是否会伤害未出生的婴儿,或正在母乳喂养或计划母乳喂养,因为不知道Trikafta是否会进入母乳。
Trikafta可能会影响其他药物的工作方式,而其他药物可能会影响Trikafta的工作方式。因此,使用某些药物时可能需要调整Trikafta的剂量。患者应特别告知医生是否服用:包括酮康唑,伊曲康唑,
泊沙康唑,
伏立康唑或氟康唑在内的抗真菌药物;抗生素包括telithromycin,clarithromycin或erythromycin;其他药物包括利福平,利福布汀,苯巴比妥,卡马西平,苯妥英钠和圣约翰草。
Trikafta可能会使某些服用它的人头晕。在知道Trikafta对他们有何影响之前,患者不应驾驶汽车,操作机械或进行任何需要警惕的事情。
服用Trikafta时,患者应避免食用含葡萄柚的食物或饮料。
Trikafta可能导致严重的副作用,包括:
血液中的肝酶高,这是用Trikafta治疗的人的常见副作用。这些可能很严重,可能是肝损伤的迹象。患者的医生将在开始Trikafta之前,在服用Trikafta的第一年中每3个月以及每年服用Trikafta时进行血液检查以检查其肝脏。如果患者出现以下肝脏问题的任何症状,应立即致电医生:右胃上部(腹部)疼痛或不适;皮肤或眼睛的白色部分发黄;食欲不振; 恶心或呕吐;尿色为琥珀色。
Trikafta治疗的某些儿童和青少年的晶状体异常(白内障)。如果患者是儿童或青少年,则其医生应在Trikafta治疗之前和期间进行眼部检查以寻找白内障。
Trikafta最常见的副作用包括头痛,腹泻,上呼吸道感染(普通感冒),包括鼻塞和流鼻涕,胃(腹部)疼痛,鼻窦发炎,肝酶增加,某种血液酶(称为肌酸磷酸激酶)增加,皮疹,流感(流感)和血液中胆红素升高。
这些并非Trikafta的所有可能的副作用。请单击此处以查看Trikafta的完整处方信息。
关于顶点
Vertex是一家全球性生物技术公司,致力于科学创新,为重症患者开发转化性药物。该公司拥有四种获批的药物,可治疗囊性纤维化(CF)的根本原因-一种罕见的,威胁生命的遗传疾病-并且在CF中有多个正在进行的临床和研究计划。除CF以外,Vertex在其他严重疾病中也拥有强大的研究药物,可深入了解人类病因生物学,例如镰状细胞病,β地中海贫血,疼痛,α-1抗胰蛋白酶缺乏症,Duchenne肌营养不良症和APOL1介导的肾脏疾病。