卡贝努瓦Cabenuva(rilpivirine和cabotegravir)HIV感染新药FDA获批
- 热度: ℃
- 来源:网络收集
- 收录时间:2021-01-23
导读:Cabenuva卡贝努瓦(rilpivirine和cabotegravir)是长效的rilpivirine(以片剂形式核准为Edurant)可注射的两种药物治疗方案,正在开发中,用于治疗成人HIV。
公司: Janssen Pharmaceuticals,Inc
.批准日期: 2021年1月21日
治疗: HIV感染
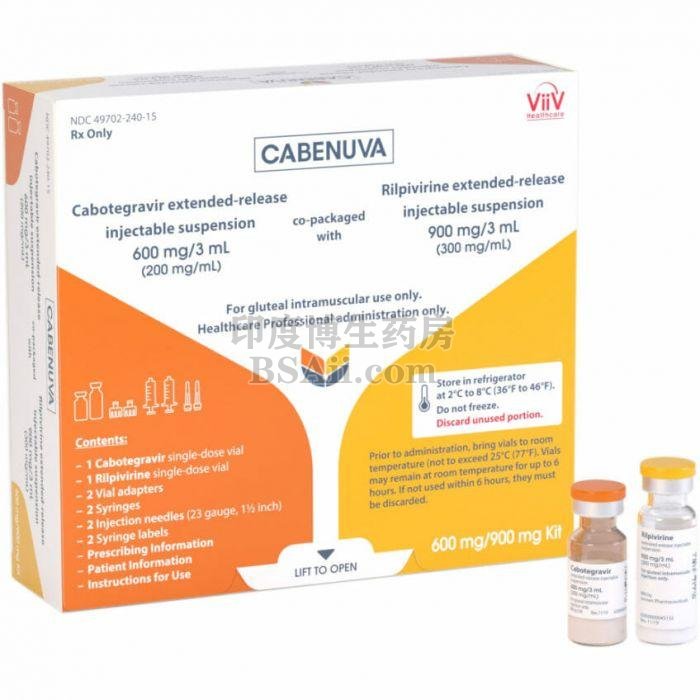
Cabenuva(rilpivirine和cabotegravir)是长效的rilpivirine(以片剂形式核准为Edurant)和研究性整合酶抑制剂Cabotegravir的每月一次,可注射的两种药物治疗方案,正在开发中,用于治疗成人HIV。
2021年1月21日,伦敦–辉瑞公司和盐野义有限公司为股东,葛兰素史克(GSK)拥有多数股权的全球专业HIV公司ViiV Healthcare今天宣布,美国食品药品监督管理局(FDA)批准了Cabenuva,治疗成人HIV-1感染的第一个也是唯一的长效方案。Cabenuva是与两种注射药物一起包装的,这两种注射药物是ViiV Healthcare的cabotegravir和Janssen的rilpivirine,每月一次,作为一种选择,可以替代目前被病毒抑制的抗逆转录病毒(ARV)方案(HIV-1 RNA小于50每毫升[mL](毫升)(毫升)),且疗程稳定,无治疗失败史,对cabotegravir或rilpivirine均无已知或怀疑耐药性。在开始治疗Cabenuva之前,1个
ViiV Healthcare北美负责人Lynn Baxter说:“今天FDA对Cabenuva的批准代表着HIV治疗方式的转变,为HIV感染者提供了一种全新的护理方法。Cabenuva将治疗剂量天数从每年365天减少到每年12天。在ViiV Healthcare,我们致力于确保没有任何人感染艾滋病毒,并将这种首创的治疗方案添加到我们行业领先的创新药物产品组合中,进一步巩固了我们的使命。”
Cabenuva的批准基于关键的III期ATLAS(抗逆转录病毒疗法作为长效抑制剂)和FLAIR(首次长效可注射疗法)研究,该研究包括来自16个国家的1,100多名患者。在开始使用卡贝诺瓦治疗之前,先给予卡波替韦和利比韦林口服治疗(导入)约一个月,以评估每种疗法的耐受性。在这些研究中,在整个48周的研究期间,每月一次肌肉内注射一次,Cabenuva在维持病毒抑制方面的效果与继续每天口服三药疗法一样有效。在这两项研究中,≥2%接受Cabenuva的临床试验参与者中观察到的最常见不良反应(1-4级)是注射部位反应,发热,疲劳,头痛,肌肉骨骼疼痛,恶心,睡眠障碍,头晕和皮疹。服用卡贝奴娃的患者中有4%(24/591)发生了严重的不良事件,而有3%(17/591)的不良事件导致停药。1个
在这些关键性研究中,相对于以前的每日口服治疗,十分之九的患者首选Cabenuva。患者偏好数据是从接受Cabenuva的临床试验参与者中收集的。在对此“意向性治疗”(ITT-E)人群进行的综合探索性分析中,有532名患者在第48周完成了一个单项问题(59名患者没有参加),88%(523/591)的人接受了Cabenuva的治疗,相比之下,两个(9/591)的人更喜欢先前的抗逆转录病毒疗法。结果本质上是描述性的,并不意味着具有临床意义。2,3
位于教堂山的北卡罗来纳大学全球健康与传染病研究所的医学教授David Wohl博士说:“在科学界中,我们认识到Cabenuva背后的创新是真正有意义的。这不仅是第一个完整的长效方案,可以大幅度减少给药频率,而且与以前的每日口服方案相比,它也是大多数临床试验参与者的首选。FDA对Cabenuva的批准强调了以社区为中心的研究的价值,我很高兴这种新的选择将为艾滋病毒携带者提供。”
为了支持向感染者(PLHIV)每月一次成功地提供治疗方案,ViiV Healthcare赞助了CUSTOMIZE试验,这是有史以来的首个预批准实施科学研究,旨在确定和评估将Cabenuva纳入临床实践的方法。美国。在AIDS2020上发表的中期调查结果表明,在四个月的时间里,大多数临床工作人员继续认为实施Cabenuva是PLHIV的高度可接受,可行和适当的方法,并且临床工作人员大大减少了他们认为实施的障碍注射方案。4
中国区首席执行官布雷特·安德鲁斯(Brett Andrews)表示:“中国为旧金山的艾滋病毒/艾滋病感染者提供法律,劳动力和行为健康服务。多年来,我们的许多客户一直在努力管理自己的健康状况,同时努力稳定自己生活中的关键方面。Cabenuva将为一些艾滋病毒携带者提供更大的自由,使其无需日常口服药物管理即可从事职业,教育和其他机会,例如旅行。长效方案是我们一直在等待的创新。”
ViiV Healthcare将在2021年2月开始向美国的批发商和专业分销商运送Cabenuva。
FDA还批准了Vocabria的新药申请(cabotegravir)30毫克(mg)口服片剂。Vocabria是与rilpivirine片联合使用的一种完整方案,适用于病毒学稳定且在稳定的ARV方案下被抑制(HIV-1 RNA小于50拷贝/ mL)的成年人中HIV-1感染的短期治疗。无治疗失败史,对cabotegravir或rilpivirine均无已知或怀疑耐药性,可在开始Cabenuva之前用作口服导入以评估cabotegravir的耐受性,以及作为可能错过计划注射Cabenuva剂量的患者的口服疗法。
关于Cabenuva(cabotegravir,rilpivirine)
Cabenuva被认为是治疗HIV感染的完整方案,这些成年人在稳定的方案中被病毒学抑制(HIV-1 RNA少于每毫升[mL] 50拷贝),且无治疗失败史,且对cabotegravir或rilpivirine无已知或怀疑耐药性。医护人员在专科诊所进行的同一次访问中,在臀部两次进行肌内注射Cabenuva(cabotegravir和rilpivirine)。
完整的方案将由ViiV Healthcare开发的整合酶链转移抑制剂(INSTI)cabotegravir与由强生的强生公司之一的Janssen Sciences Ireland UC开发的非核苷逆转录酶抑制剂rilpivirine(NNRTI)结合在一起。Rilpivirine在美国被批准为25毫克片剂,每天服用一次,与12岁及12岁以上的未接受抗逆转录病毒治疗的患者联合使用其他抗逆转录病毒药物与其他抗逆转录病毒药物联合治疗,体重至少35千克,病毒载量≤100,000 HIV RNA拷贝/ mL。
像cabotegravir一样,INSIT可以通过阻止病毒DNA整合到人类免疫细胞(T细胞)的遗传物质中来抑制HIV复制。此步骤在HIV复制周期中必不可少,并且还负责建立慢性感染。Rilpivirine是一种NNRTI,其通过干扰一种称为逆转录酶的酶起作用,从而阻止病毒繁殖。
商标归ViiV Healthcare集团公司所有或许可。
关于ATLAS和FLAIR
ATLAS(NCT02951052)是一项III期,开放标签,主动控制,多中心,平行组,非劣效性研究,旨在评估长效,可注射的Cabotegravir和rilpivirine两种药物疗法的抗病毒活性和安全性与病毒抑制个体中两种核苷逆转录酶抑制剂(NRTIs)加上整合酶抑制剂(INI),NNRTI或蛋白酶抑制剂(PI)的当前口服ARV持续剂量相比,每四周服用一次。ATLAS的主要终点是在第48周时按照FDA快照算法,血浆HIV-1 RNA≥50c / mL的参与者所占的比例(缺少,转换或中止=失败,ITT-E人群)。在第一个或第二个疗程中,受试者必须被病毒抑制六个月或更长时间,且无先前的失败。
ATLAS包括616名艾滋病毒感染者,目前正在阿根廷,澳大利亚,加拿大,法国,德国,意大利,墨西哥,俄罗斯,南非,韩国,西班牙,瑞典和美国的研究中心进行。
FLAIR(NCT02938520)是一项III期,随机,开放标签,多中心,平行组,非劣效性研究,旨在评估肌内,长效,可注射的Cabotegravir和rilpivirine两种药物疗法的抗病毒活性和安全性在经过Triumeq(abacavir /
dolutegravir / lamivudine)的诱导治疗20周后,被病毒抑制的成人HIV感染者。FLAIR的主要终点是在第48周时,根据FDA快照算法,血浆HIV-1 RNA≥50c / mL的参与者所占的比例(缺少,转换或中止=失败,ITT-E人群)。
FLAIR包括566名艾滋病毒感染者,正在加拿大,法国,德国,意大利,日本,荷兰,俄罗斯,南非,西班牙,英国和美国的研究中心进行研究。
Cabenuva重要安全信息
Cabenuva被认为是治疗成人人类1型免疫缺陷病毒(HIV-1)感染的完整方案,以替代目前在病毒学上被抑制(HIV-1 RNA少于50拷贝/ mL)的人的现有抗逆转录病毒疗法。稳定的抗逆转录病毒疗法,无治疗失败史,对cabotegravir或rilpivirine均无已知或怀疑耐药性。
禁忌症
先前对cabotegravir或rilpivirine过敏反应的患者请勿使用Cabenuva。
接受卡马西平,奥卡西平,苯巴比妥,苯妥英钠,利福布汀,利福平,利福喷丁,全身性地塞米松(> 1剂)和圣约翰草的患者,请勿使用卡贝努瓦。
警告和注意事项:
过敏反应:
含有利比韦林的方案上市后的经验表明,有超敏反应,包括与嗜酸性粒细胞增多症和全身症状的药物反应病例。虽然一些皮肤反应伴有发烧等体质症状,但其他皮肤反应与器官功能障碍有关,包括肝血清生化指标升高。
据报道与其他整合酶抑制剂相关的严重或严重的超敏反应,可能与Cabenuva发生。
如果出现超敏反应的体征或症状,请立即停用Cabenuva。应监测临床状况,包括肝转氨酶,并开始适当的治疗。在给予Cabenuva之前开处方口服引入药物,以帮助识别可能有超敏反应风险的患者。
注射后反应:
注射利必韦林后几分钟内就出现了严重的注射后反应(报道的受试者不到1%),包括呼吸困难,躁动,腹部绞痛,潮红,出汗,口腔麻木和血压变化。这些事件可能与不经意的(部分)静脉内给药有关,并在注射后数分钟内开始缓解。
在准备和给药Cabenuva时,请仔细遵循使用说明,以免意外静脉注射。注射后短暂(约10分钟)观察患者。如果发生注射后反应,请按照临床指示进行监测和治疗。
肝毒性:
据报道,接受卡波可韦或利必韦林治疗的患者中,有或没有已知的预先存在的
肝病或可确定的危险因素,均具有肝毒性。
治疗前患有基础
肝病或转氨酶水平明显升高的患者,转氨酶升高或发展的风险可能更高。
建议对肝化学进行监测,如果怀疑有肝毒性,应停止用卡贝诺娃治疗。
抑郁症:
Cabenuva或个别产品已报告有抑郁症(包括情绪低落,抑郁,重度抑郁,情绪改变,情绪波动,烦躁不安,消极想法,自杀意念或企图)。
及时评估有抑郁症状的患者。
由于药物相互作用而产生不良反应或病毒学应答丧失的风险:
Cabenuva和其他药物的并用可能会导致已知或潜在的重大药物相互作用(请参阅禁忌症和药物相互作用)。
Rilpivirine的剂量比推荐的口服剂量高3到12倍,可以延长QTc间隔。Cabenuva应谨慎与已知有Torsade de Pointes风险的药物结合使用。
Cabenuva的长效特性和潜在的相关风险:
Cabotegravir和rilpivirine的残留浓度可能会长时间(最多12个月或更长时间)保留在患者的全身循环中。选择适合所需每月注射剂量方案的合适患者,因为不遵守每月注射剂量或错过剂量可能会导致病毒学应答丧失和耐药性发展。
为了最大程度地降低发生病毒抗药性的潜在风险,必须在Cabenuva的最终注射剂量后不迟于1个月内启动另一种完全抑制性抗逆转录病毒疗法。如果怀疑是病毒学衰竭,请尽快将患者改用其他治疗方案。
不良反应
卡贝努瓦最常见的不良反应(发生率≥2%,所有等级)是注射部位反应,发热,疲劳,头痛,肌肉骨骼疼痛,恶心,睡眠障碍,头晕和皮疹。
药物相互作用
有关Cabenuva,Vocabria或rilpivirine的重要药物相互作用,请参阅适用的完整处方信息。
由于Cabenuva是一种完整的治疗方案,因此不建议与其他抗逆转录病毒药物共同给药治疗HIV-1感染。
作为UGT1A1或1A9的强诱导剂的药物有望降低cabotegravir的血浆浓度。诱导或抑制CYP3A的药物可能会影响rilpivirine的血浆浓度。
Cabenuva应谨慎与已知有Torsade de Pointes风险的药物结合使用。
在特定人群中的使用
怀孕:关于怀孕期间使用卡贝诺娃的人类数据不足,不足以充分评估与药物相关的先天缺陷和流产风险。讨论在怀孕和怀孕期间使用Cabenuva的益处风险,并考虑在停止注射Cabenuva后长达12个月或更长时间在全身循环中检出cabotegravir和rilpivirine。已经建立了抗逆转录病毒妊娠登记库。
哺乳期:疾病预防控制中心建议美国的HIV-1感染母亲不要母乳喂养婴儿,以免冒产后传播HIV-1感染的风险。不建议使用母乳喂养,因为可能会在HIV阳性婴儿中发展出病毒抗药性,在母乳喂养婴儿中产生不良反应,并且在停止注射卡贝诺韦后长达12个月或更长时间在全身循环中可检测到卡波韦韦和利比韦林的浓度。
请查看完整的处方信息。
重要的Vocabria安全信息
Vocabria是一种人类免疫缺陷病毒1型(HIV-1)整合酶链转移抑制剂(INSTI),与rilpivirine结合使用可短期治疗在病毒学上被抑制的成人HIV-1感染(HIV-1 RNA小于50稳定的抗逆转录病毒疗法,无治疗失败史,对cabotegravir或rilpivirine无已知或怀疑耐药性,用于:
口服前评估Cabenuva(cabotegravir; rilpivirine)缓释注射混悬液给药前对cabotegravir的耐受性。
口服治疗,将错过计划的Cabenuva注射剂量的患者。
禁忌症
先前对Cabotegravir的超敏反应。
与卡马西平,奥卡西平,苯巴比妥,苯妥英钠,利福平和利福喷丁共同给药。
警告和注意事项
据报道超敏反应与其他整合酶抑制剂有关。如果出现超敏反应的体征或症状,请立即中止词汇。
有报道称接受卡博可韦的患者有肝毒性。建议监测肝化学成分。如果怀疑有肝毒性,请中止词汇。
据报道,Vocabria患有抑郁症。建议对抑郁症状进行及时评估。
联合治疗相关的风险:在开始与rilpivirine结合使用Vocabria之前,应先阅读rilpivirine的处方信息。
不良反应
至少在接受Vocabria的3位受试者中观察到最常见的不良反应(1-4级)为头痛,恶心,梦境异常,焦虑和失眠。
药物相互作用
有关与Vocabria的重要药物相互作用,请参阅完整的处方信息。
由于Vocabria与rilpivirine联用是一种完整的治疗方案,因此不建议与其他抗逆转录病毒药物并用以治疗HIV-1感染。
诱导尿苷二磷酸葡萄糖醛糖基转移酶(UGT)1A1的药物可能会降低cabotegravir的血浆浓度。
在特定人群中的使用
哺乳期:由于可能传播HIV-1,因此不建议母乳喂养。
关于ViiV Healthcare
ViiV Healthcare是全球专业的艾滋病毒公司,由葛兰素史克(LSE:GSK)和辉瑞(NYSE:PFE)于2009年11月成立,致力于为艾滋病毒感染者和有感染风险的人提供治疗和护理方面的进步艾滋病病毒。Shionogi于2012年10月加入。该公司的目标是对艾滋病毒/艾滋病的兴趣比以往任何一家公司都更加深刻和广泛,并采取一种新方法来提供有效和创新的药物来治疗和预防艾滋病毒,并支持受影响的社区通过艾滋病毒。有关公司,其管理,产品组合,渠道和承诺的更多信息,请访问www.viivhealthcare.com。
关于ViiV Healthcare的患者援助计划
ViiV Healthcare致力于为美国需要我们的药物的合格HIV感染者提供帮助。ViiV Healthcare的集中式服务ViiV Connect提供有关访问和覆盖范围的全面信息,以帮助居住在美国的患者获得规定的ViiV Healthcare药品,而无论这些药品是否已投保,未投保或未投保。ViiV Connect提供了专用访问协调器的一对一支持,并拥有一个集成的网站,一个拥有很多资源的网站,包括一个门户。
关于葛兰素史克
GSK是一家以科学为主导的全球医疗保健公司,其宗旨是:帮助人们做更多,感觉更好,寿命更长。
关于前瞻性陈述的警告性声明
GSK告诫投资者,GSK所作的任何前瞻性陈述或预测(包括本公告中的陈述或预测)都将承受可能导致实际结果与预期产生重大差异的风险和不确定性。此类因素包括但不限于公司2019年20-F年度报告中第3.D节“风险因素”中所述的因素,以及GSK第三季度业绩的“主要风险和不确定性”部分中列出的因素以及COVID-19大流行的任何影响。
卡贝诺娃(cabotegravir,rilpivirine)处方信息。2021年1月
获得美国批准。2.Swindells S,Andrade-Villnueva JF,里士满GJ等。长效Cabotegravir和Rilpivirine用于维持HIV-1抑制。新英格兰医学杂志,382(12),1112-1123。https://doi.org/10.1056/nejmoa1904398。
3.Orkin C,ArastéhK,Hernández-MoraMG等。口服诱导HIV 1感染后的长效卡博格韦和利吡韦林。《新英格兰医学杂志》 382(12),1124–1135。https://doi.org/10.1056/nejmoa1909512
4,Czarnogorksi M,Garris C,Wannamaker P等。在美国医疗机构中,Cabotegravir和Rilpivirine长效(CAB + RPV LA)的实施科学混合III研究(CUSTOMIZE)的初始阶段,感知的实施障碍会减少:在2020年第23届国际艾滋病大会上发表。
资料来源:ViiV Healthcare
发表于:2021年1月