
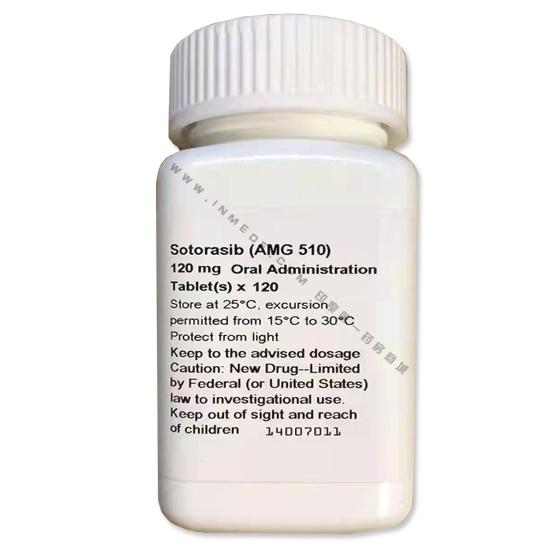
sotorasib商品名为:Lumakras 研发代号:AMG510 中文译为:索托拉西布 该药是RAS GTPase家族的一种抑制剂,适用于治疗KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)(经FDA批准的检测确定)的成年患者,这些患者至少接受过一次既往全身治疗。

推荐剂量:每日一次,口服960mg。
吞下整粒药片,可与食物同服,也可不与食物同服。
(警告)本内容仅供参考,不能替代医嘱
最常见的不良反应(≥ 20%)为腹泻、肌肉骨骼疼痛、恶心、疲劳、肝毒性和咳嗽。最常见的实验室检测异常(≥ 25%)为淋巴细胞减少、血红蛋白减少、天冬氨酸转氨酶增加、丙氨酸转氨酶增加、钙减少、碱性磷酸酶增加、尿蛋白增加和钠减少。
(警告)本内容仅供参考,不能替代医嘱
2021年02月17日讯 / --安进(AMGEN)近日宣布,美国食品和药物管理局(FDA)已受理靶向抗癌药sotorasib(AMG 510)的新药申请(NDA)并授予了优先审查,该药是一种KRASG12C抑制剂,用于治疗先前已接受过至少一种系统疗法、经FDA批准的检测方法证实存在KRAS G12C突变、局部晚期或转移性非小细胞肺癌(NSCLC)患者。根据优先审查,sotorasib NDA的《处方药用户收费法》(PDUFA)目标日期为2021年8月16日,较标准审查周期缩短4个月。2020年12月初,FDA授予了sotorasib突破性药物资格(BTD)和实时肿瘤学审查资格(RTOR)。2021年1月底,sotorasib获得了中国国家药品监督管理局(NMPA)药品审评中心(CDE)授予突破性治疗药物资格。这是安进首次在中国提交“突破性治疗药物”认证申请,同时也是与百济神州达成战略合作以来的首个“突破性治疗药物”认证申请。安进于2020年12月16日向美国FDA提交了sotorasib的NDA。目前,该机构正在RTOR试点项目下对该NDA进行评估。RTOR项目旨在探索一种更有效的审查程序,以确保尽早向患者提供安全有效的治疗。2020年12月,安进向欧洲药品管理局(EMA)提交了营销授权申请(MAA)。此外,在2021年1月,安进向澳大利亚、巴西、加拿大、英国提交了MAA。sotorasib是第一个进入临床开发的KRAS G12C抑制剂,现在,该药有潜力成为第一个被批准用于治疗携带KRAS G12C突变的晚期NSCLC患者的靶向疗法。在美国,大约13%的NSCLC患者携带KRAS G12C突变,面临着严重未满足的医疗需求。
sotorasib的上市申请,基于II期CodeBreaK 100研究中晚期NSCLC患者队列的阳性结果,这些患者先前接受化疗和/或免疫疗法后病情进展。该研究的完整结果已在2020年第21届世界肺癌大会(WCLC)线上会议上公布,数据显示,:在先前接受过化疗和/或PD-1/PD-L1免疫疗法治疗病情进展的KRAS G12C突变晚期NSCLC患者中,sotorasib显示出持久的抗肿瘤活性和积极的益处风险特征:确认的客观缓解率(ORR)为37.1%、疾病控制率(DCR)为80.6%、中位缓解持续时间(DOR)为10个月、中位无进展生存期(PFS)为6.8个月。探索性分析显示,在一系列生物标志物亚组中观察到对sotorasib令人鼓舞的肿瘤反应,包括PD-L1表达水平阴性或水平低的患者和STK11突变的患者。这种共突变与接受检查点抑制剂和化疗的NSCLC患者的不良预后相关。目前,安进正在开展一项全球3期随机、阳性对照研究(CodeBreaK 200),在KRAS G12C突变NSCLC患者中,将sotorasib与多西紫杉醇化疗进行对比。
KRAS G12C是NSCLC中最常见的KRAS突变。在美国,约13%的NSCLC腺癌患者存在KRAS G12C突变,每年约有25000例新患者被诊断为携带KRAS G12C突变的NSCLC。对于接受一线治疗失败的KRAS G12C突变NSCLC患者,治疗选择非常有限,存在着非常高的未满足医疗需求。针对二线KRAS G12C突变NSCLC患者,当前疗法的效果并不理想,缓解率在9-18%,中位无进展生存期(PFS)仅约4个月。KRAS是被发现的首批癌基因中的一种,其突变存在于大约1/4的人类肿瘤中,是肿瘤学药物研发领域最明确的靶标之一。然而遗憾的是,尽管前景很好,但KRAS长期以来几乎无法攻克,这是由于该蛋白是一种无特征、近乎球形的结构,无明显的结合位点,很难合成一种能靶向结合并抑制期活性的化合物。目前,KRAS已成为肿瘤药研发领域“不可成药”靶标的代名词。sotorasib(AMG 510)是成功靶向KRAS并进入人体临床开发的首批小分子抑制剂之一,可靶向抑制携带G12C突变的KRAS蛋白。sotorasib通过将G12C突变KRAS蛋白锁定在一种非激活GDP结合状态来特异性地和不可逆地抑制其促增殖活性。通过开发sotorasib,安进承接了过去40年来癌症研究中最严峻的挑战之一。sotorasib是第一个进入临床的KRASG12C抑制剂,目前正在进行一项最广泛的临床项目CodeBreaK,在全球4大洲探索10种药物组合。在短短2年多的时间里,CodeBreaK项目还建立了最深入的临床数据集,对13种肿瘤类型的600多例患者进行了研究。
原文出处:FDA Grants Sotorasib Priority Review Designation For The Treatment Of Patients With KRAS G12C-Mutated Locally Advanced Or Metastatic Non-Small Cell Lung Cancer
(警告)本内容仅供参考,不能替代医嘱