
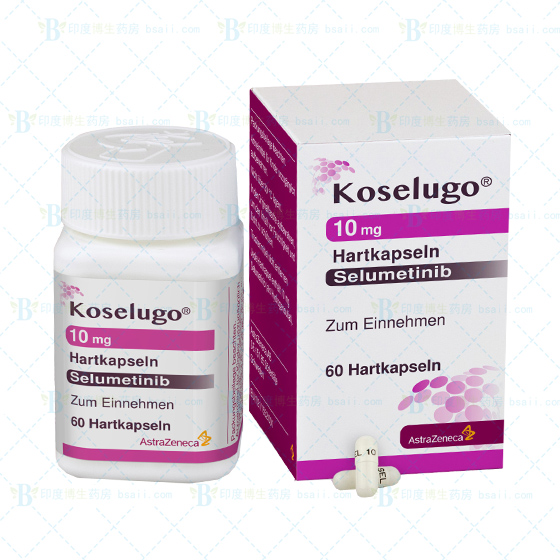
Koselugo(Selumetinib)司美替尼 是一种靶向MEK的激酶抑制剂(TKI),MEK是RAS/MAPK信号通路中的关键蛋白激酶。Koselugo能够选择性地抑制MEK1和MEK2,从而让失调的信号通路恢复正常,进而缓解儿童NF1患者的病情。

该成品药物剂型为10mg和25mg的胶囊。服用方法是空腹,25mg/m2每天二次
(警告)本内容仅供参考,不能替代医嘱
最常见的毒副反应为是皮疹(75%),其次是腹泻(58%)、恶心(44%)、疲劳(39%)和周围水肿(33%)。12%的病人有短暂的和可逆的视力模糊。这些不良反应大多为1级或2级。
(警告)本内容仅供参考,不能替代医嘱
2020年4月10日美国FDA宣布批准阿利斯康(AstraZeneca)公司和默沙东(MSD)公司共同开发的Koselugo(selumetinib)司美替尼上市,治疗2岁及2岁以上的1型神经纤维瘤病(NF1)儿童患者,这些患者携带有表现出症状和/或进行性,不能通过手术治疗的丛状神经纤维瘤(PN)。除了治疗上述疾病外,下面给大家八一八司美替尼在治疗肺癌上的临床上应用。
MEK抑制剂司美替尼药物介绍
Selumetinib (司美替尼)(ARRY-142886 ; AZD6244)是一种可口服的、选择性的、非竞争性的ATP活性的MEK1/2抑制剂,在RAF和RAS下游抑制MAP/ERK通路。MAP/ERK通路是肿瘤增长的重要调节机制,变异RAS、RAF也被公认是致癌基因,恶性黑素瘤有50%BRAF变异,肺癌有~25%KRAS变异,但是抑制MEK却相当复杂。
该成品药物剂型为10mg和25mg的胶囊。服用方法是空腹,25mg/m2每天二次,最常见的毒副反应为是皮疹(75%),其次是腹泻(58%)、恶心(44%)、疲劳(39%)和周围水肿(33%)。12%的病人有短暂的和可逆的视力模糊。这些不良反应大多为1级或2级。
Selumetinib(司美替尼)可能的临床适应症
1)治疗神经纤维瘤病患者的神经纤维瘤。
2)BRAF激活突变:除甲状腺癌外,在黑色素瘤(高达59%),结直肠癌(5-22%),浆液性卵巢癌(高达30%)、肺癌和其他几种肿瘤类型中普遍存在。
3)GNAQ突变:Selumetinib也被证明可抑制GNAQ突变的葡萄膜黑色素瘤细胞系的生长。此外,初步结果表明,selumetinib治疗葡萄膜黑色素瘤患者可导致肿瘤缩小,这是持续抑制ERK 磷酸化的结果。
4)KRAS突变:出现在20%至30%的NSCLC非小细胞肺癌病例和约40%的结肠直肠癌中。MEK抑制剂通路介绍
MEK这个靶点很多患者朋友从未听过,但其所在的MAPK通路是非常有名气的,参与了包括非小细胞肺癌在内的多种癌症的肿瘤发生。研究表明RAS—RAF—MEK—ERK信号通路是重要的细胞内信号传递通路,该通路形成上下游信号传递通路,存在于大多数细胞中,且与多种细胞功能相关,可参与细胞运动、凋亡、分化及生长增殖等多种生理过程,特别是肿瘤细胞。但当该通路上基因发生突变而活化时,该通路会被异常持续激活,导致细胞增殖不受限,而形成肿瘤细胞,而我们各癌种中常见的KRAS、BRAF的突变就基于该通路。
MEK分为MEK1/2属于一种丝、苏氨酸蛋白激酶,它可激活ERK,是RAS与RAS的下游应答因子,抑制MEK的活性可以阻断下游通路的方式实现上游基因变异引起的异常活化,从而发挥抗肿瘤作用。KRAS在肺腺癌的发生率为20%-30%,BRAF在肺腺癌的发生率为2%-4%,MEK1在肺腺癌的发生率为0.6%。
临床研究数据:KRAS突变肺癌患者癌
KRAS突变在肺癌里非常常见,肺腺癌里的KRAS突变频率约为25%鳞癌里KRAS基因突变频率为5%。直接针对KRAS突变的靶向药物目前还没有,思路是打击KRAS基因下游的MEK靶点。
1.初期探索,单药失利。
司美替尼单药治疗KRAS、NRAS、HRAS或BRAF突变的肺癌患者,疗效有限未能达到主要疗效终点。在一项包含非小细胞肺癌、小细胞肺癌和胸腺恶性肿瘤患者的篮子试验中,对于KRAS、NRAS、HRAS或BRAF突变的患者采用司美替尼单药治疗。在9例可评估的NSCLC患者中,只有11%患者达到PR,中位PFS为2.3个月,中位OS为6.5个月,未达到主要疗效终点。11例RAS/RAF突变的患者接受了司美替尼治疗。未能达到主要疗效终点。提示单药MEK,对于该通路基因突变驱使的肺癌治疗是不可行的。机制分析可能存在旁路活化的可能。也因此引发了MEK抑制剂联合其他治疗策略的探讨。
2. 尝试联合策略,初显成效。
一项多中心、11期、随机安慰剂对照临床试验中,司美替尼联合多西他赛治疗KRAS突变NSC纳入的患者按1:1的比例随机分为试验组和对照组,试验组接受多西紫杉醇(75mg/m2,dl,q21d)联合口服司美替尼胶囊(75 mgbid),预期6个周期;对照组接受安慰剂联合多西紫杉醇治疗。直到疾病进展或者出现不可耐受的毒性反应。研究中司美替尼可进行三阶段的减量:75mg qd(第一次减量),50 mg bid(齐i]量调整),50 mgqd(最终的减量)。一旦减量或者调整将不再调回原剂量。
主要结果:共人组患者87例(试验组44例,对照组43例)。中位随访时间7.2个月,司美替尼联合多西紫杉醇组的OS较对照组长(9.4个月VS5.2个月,风险比0.8,P=O.21)。所有的次要终点指标,包括中位PFS(5.3个月VS 2.1个月,风险比0.58,P=0.014),6个月内无进展生存率(37.1%VS15.8%),ORR(37%VS0%),均显示司美替尼联合多西紫杉醇组优于单用多西紫杉醇组。对主要的安全性数据统计分析后发现,司美替尼联合多西紫杉醇组与单用多西紫杉醇组发生3度以上不良反应分别为82%和67%.其中发生最多的是粒缺性发热,发生率分别为14%和0%。司美替尼联合多西紫杉醇组常见非血液系统不良反应包括腹泻(73%)、恶心(43%)、呕吐(43%)、周围性水肿(41%)、口腔炎(36%)、食欲减退(34%)等。
结论:在二线治疗KRAS突变的NSCLC方案中.司美替尼联合多西紫杉醇虽然在统计学意义上未能明显提高0S,具有更多的不良反应:但能显著延长患者的PFS、提高有效率。以此为基础的进一步临床试验值得期待。
3.三阶段验证联合策略,疗效提升,但未达到主要研究终点。
司美替尼联合多西他塞相比单独多西没有改善主要研究终点PFS。尽管二阶段的研究取得了有希望的结果,但在510例晚期KRAS突变NSCLC(SELEC
T-1) 三阶段随机随访中,尽管这项研究与二阶段试验设计相同,司美替尼联合多西他塞相比单独多西没有改善主要研究终点PFS。两组OS也无差异 (8.7个月对比7.9个月 ), 司美替尼组ORR为20.1%,安慰剂组为13.7%。司美替尼和多西紫杉醇的副作用与二阶段试验总体上相似,但由于强制使用粒细胞集落刺激因子,第三阶段试验中中性粒细胞减少和发热性中性粒细胞减少的情况比二阶段试验少。为什么司美替尼组第三阶段的研究中表现不佳目前尚不清楚。
临床研究数据:KRAS突变卵巢癌患者
低级别浆液性卵巢癌的一线治疗策略是手术继以放疗。但是,这种肿瘤生长缓慢,对传统化疗药物反应不佳。由于低级别浆液性卵巢癌被证明存在MEK基因突变,研究使用司美替尼靶向药促分裂原活化蛋白激酶(MAPK)通路的MEK1/2蛋白激酶。
GOG的研究人员给予52例患者100mg司美替尼,口服,每日2次,4周为1周期的治疗,33%的患者接受了12个或更多周期的治疗。研究开始之前,58%的患者已经接受了3轮或以上的化疗。
司美替尼使81%的患者疾病得到控制。尤其是,8例患者得到完全或部分缓解,34例疾病稳定。中位无进展生存期为11个月,63%的患者无进展生存期超过6个月。此外,患者对司美替尼耐受性良好,仅3例患者发生4级不良事件。临床研究数据:BRAFV600E突变黑色素瘤
临床实验RO4987655 (CH4987655)是一个最近在进行I期临床试验评估的MEK抑制剂,8例NRAS突变黑色素瘤患者中,1例部分缓解PR(13%),2例病情稳定(25%)。
该病例患者26岁女性,确诊黑色素瘤IIIb期后,进行了局部的切除,3年后出现了颈部局部的复发、淋巴结和胸壁的转移。基因检测显示BRAFV600E的突变,后续进行达卡巴嗪治疗失败后,开始进行司美替尼75mg,bid的治疗。治疗数周后,患者胸壁肿瘤和颈部淋巴结病灶消退,变扁平,消失。在治疗4个月后,疗效评价完全缓解(CR)。总结
大批MEK抑制剂相关临床试验在开展,方向多样化,期待更多利好的临床研究结果出现!
(警告)本内容仅供参考,不能替代医嘱